Variantes “naturales” de EPO
Un proyecto conjunto de Sanofi-Aventis y la empresa americana Transkaryotic Therapies (adquirida en 2005 por el productor farmacéutico británico Shire Pharmaceuticals) ha logrado obtener EPO generada por células humanas transformadas mediante activación genética (la línea HT-1080, células aisladas del fibrosarcoma), bajo el nombre comercial DynEpo (Epoetina δ). La empresa Shire publicó por primera vez en Septiembre de 2006 sus exitosos resultados en estudios de fase III. Dynepo se comercializa ya en el mercado alemán desde el 15 de Marzo de 2007.
La empresa biotecnológica francesa Odyssey ha descubierto una variante natural de EPO marcada por SNP que muestra una actividad superior al 30-50% en experimentos in vitro con respecto a la EPO nativa. La variante se ha llamado “GO-EPO” y se debe al intercambio de un único aminoácido en la estructura terciaria, un cambio de configuración cercano al lugar de conexión del receptor de la EPO que aumenta claramente la afinidad de la molécula por el receptor.
La compañía americana GlycoFi ha logrado generar EPO humana en levaduras del género Pichia (P. pastoris). La glicosilación específica para la levadura podría ser evitada por la modificación post-translacional mediante la introducción de elementos genéticos así como secuencias genéticas específicas de los humanos en las células de levadura. En Mayo de 2006 GlycoFi fue adquirida por la farmacéutica estadounidense Merck & Co.
Miméticos de EPO
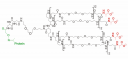 La compañía biofarmacéutica Gryphon Therapeutics, residente en San Francisco (anteriormente Gryphon Sciences) ha desarrollado la primera proteína de eritropoyésis sintética (SEP). La SEP es una macromolécula totalmente sintética que consiste de un polipéptido con 166 monómeros de aminoácido que muestra una alta homología secuencial con la molécula nativa de EPO. Este polipéptido contiene dos monómeros de Lisina no naturales (Lys 24 y Lys 126, ambas Nε-levulinilo) sobre los cuales está enlazado un polímero de longitud definida cargado negativamente. La actividad de la SEP in vitro es comparable con la de la EPO, pero su duración media en suero es aproximadamente 2.5 veces mayor. En 2002, Hoffmann-La Roche adquirió la licencia para la aplicación de la proteína en los tratamientos clásicos de la EPO.
La compañía biofarmacéutica Gryphon Therapeutics, residente en San Francisco (anteriormente Gryphon Sciences) ha desarrollado la primera proteína de eritropoyésis sintética (SEP). La SEP es una macromolécula totalmente sintética que consiste de un polipéptido con 166 monómeros de aminoácido que muestra una alta homología secuencial con la molécula nativa de EPO. Este polipéptido contiene dos monómeros de Lisina no naturales (Lys 24 y Lys 126, ambas Nε-levulinilo) sobre los cuales está enlazado un polímero de longitud definida cargado negativamente. La actividad de la SEP in vitro es comparable con la de la EPO, pero su duración media en suero es aproximadamente 2.5 veces mayor. En 2002, Hoffmann-La Roche adquirió la licencia para la aplicación de la proteína en los tratamientos clásicos de la EPO.
Actualmente la compañía americana Affymax desarrolla un preparado con el nombre de Hematide que está en fase clínica II. Además, investiga otro polipéptido cuyo impacto se corresponde con el de la EPO nativa (análogo de EPO) pero cuya secuencia de aminoácidos, sin embargo, no tiene homología con la molécula de EPO nativa. Además, para evitar una rápida eliminación por los riñones se utiliza el péptido de estabilización PEG (como el CERA de Hoffmann-La Roche). Su efectividad ya se ha demostrado en ensayos con animales. Según los resultados de Affymax, el tratamiento para la anemia con este preparado duraría solo de tres a cuatro semanas.
La firma canadiense ProMetic Biosciences ha desarrollado el “PBI-1402”, un análogo de EPO que ha mostrado efectos estimulantes y antiapoptósicos en la formación de eritrocitos y granulocitos, en estudios clínicos de fase I.
Bajo la denominación de “PT-401”, la empresa DNAPrint Genomics, residente en Florida, trabaja actualmente en estudios preclínicos sobre un dímero de EPO que debería tener una mayor afinidad con el receptor de EPO que la EPO nativa.
La empresa biofarmacéutica alemana AplaGen ha desarrollado un mimético de la EPO en el cual el péptido funcional está acoplado a una macromolécula. Como ocurre con las moléculas de PEG, la eliminación por los riñones es menor debido al aumento de tamaño de la molécula. Actualmente el preparado está en estudios clínicos de fase I y puede aplicarse por vía intravenosa y parenteral, aunque están estudiándose otras formas de presentación.
•La vida media de eliminación de metoxi-polietilenglicol epoetina beta tras la administración intravenosa o subcutánea es la misma; la vida media de eliminación de metoxi-polietilenglicol epoetina beta es > 20 veces más prolongada que la vida media notificada para la epoetina alfa y seis veces más prolongada que la de la darbepoetina alfa administrada por vía intravenosa. •Metoxi-polietilenglicol epoetina beta está indicado para el tratamiento de la anemia relacionada con la ERC en pacientes dializados y en pacientes sin dializar.